新闻网讯(通讯员熊天晨、张志东)11月2日,生命科学学院/免疫与代谢前沿科学中心/医学研究院钟波教授课题组在国际期刊Nature Communications(《自然·通讯》,IF:12.131)上在线发表论文,阐述了E3泛素连接酶RNF115在RNA和DNA病毒感染的不同时期分别催化MAVS和MITA发生不同类型的泛素化,从而分别抑制和促进抗RNA病毒以及抗DNA病毒免疫应答。
论文题为“RNF115 plays dual roles in innateantiviral responses by catalyzing distinct ubiquitination of MAVS and MITA”的学术论文。生命科学学院2018级博士研究生张志东和医学研究院2018级博士研究生熊天晨为该论文共同第一作者。
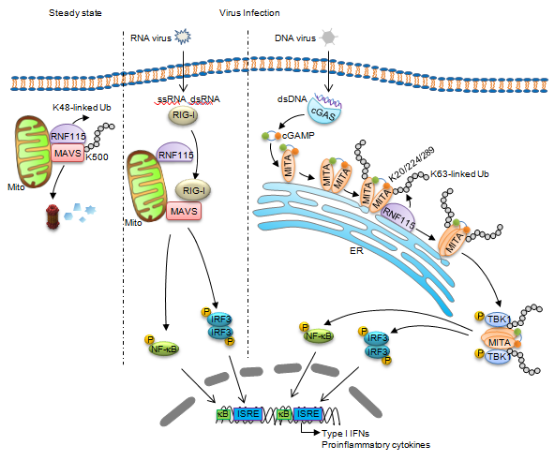
天然免疫是保护机体抵御病原微生物的入侵的第一道生理防线。其中VISA(也称MAVS)和MITA(也称STING)介导的信号通路在机体抗RNA和DNA病毒天然免疫应答过程中扮演着重要角色,其功能受到多种翻译后修饰的严格调控,如泛素化、苏素化、磷酸化等。
该研究小组发现在未受感染的细胞中,RNF115持续催化MAVS发生K48位链接的多聚泛素化修饰,使其通过蛋白酶体途径降解从而阻止过度的I型干扰素表达;在DNA病毒HSV-1感染细胞后,RNF115催化MITA发生K63位链接的泛素化修饰,从而促进MITA的寡聚化以及对下游蛋白激酶TBK1的招募和I型干扰素的表达。
进一步的研究结果表明,RNF115基因敲除小鼠对RNA病毒EMCV更加抵抗而对DNA病毒HSV-1更加易感。该研究阐明了E3泛素连接酶RNF115调控RNA和DNA病毒感染诱导I型干扰素表达的分子机制,同时揭示了MAVS与MITA在病毒感染的不同时空发生泛素化修饰的新机制,推动了我们对抗病毒天然免疫反应机理的理解。
该项研究受到国家重点研发计划、国家自然科学基金、湖北省自然科学基金以及武汉大学医学腾飞计划与自主科研项目等项目的支持。
据悉,钟波课题组主要研究感染免疫、炎性疾病与肿瘤发生的分子机制与靶向治疗。自2013年以来,钟波课题组发现了多个调控上述过程的关键蛋白,并解析了其分子机制,已在Cell Research、Nature Cancer、Cell Host Microbe、Nature Communications、JEM、PNAS等国际知名期刊发表论文17篇,这些研究为未来相关疾病的治疗提供了分子靶标与理论基础,受到国内外同行的广泛关注。
(编辑:陈丽霞)