新闻网讯(通讯员许艳)近日,《德国应用化学》(Angew. Chem. Int. Ed.)以通讯(communication)形式,在线发表化学与分子科学学院教授、高等研究院兼职研究员周强辉团队在活性天然产物全合成方面的最新研究成果。
论文题为“一种结构多样性导向合成1,3-反式二取代四氢异喹啉的模块化方法:Michellamines B和C的七步不对称全合成”(A Modular Approach for Diversity-Oriented Synthesis of 1,3-trans-Disubstituted Tetrahydroisoquinolines: Seven-Step Asymmetric Synthesis of Michellamines B and C)。化学与分子科学学院2018级博士生白淼为第一作者,周强辉为通讯作者。此外,2020级硕士生贾仕虎、2016级本科生张旌扬,以及程鸿刚老师为本文的研究做出了重要贡献,武汉大学丛恒将老师和刘珊珊老师在样品测试表征方面提供了重要帮助,大赛璐手性技术(上海)有限公司为关键中间体的分离纯化做出了重要贡献。
1,3-反式二取代四氢异喹啉是一类非常重要的杂环化合物,含有该结构的活性天然产物超过100种。此外,礼来公司开发的二期临床药物D1-阳性变构调节剂(PAM)mevidalen的分子核心骨架就是1,3-反式二取代四氢异喹啉。因此,发展1,3-反式二取代四氢异喹啉的高效合成方法具有重要意义。
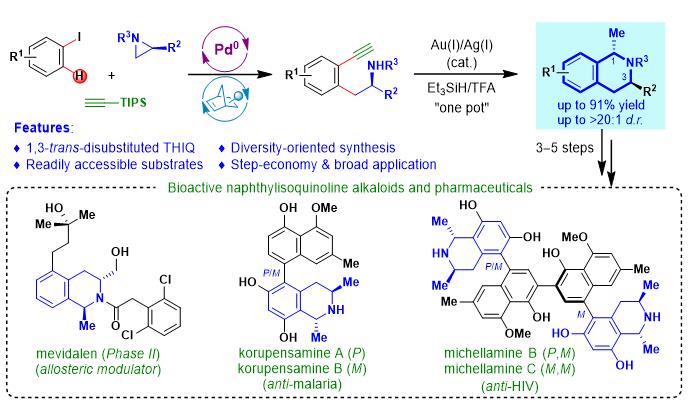
近年来,周强辉团队聚焦于Pd/NBE协同催化策略开发多取代芳烃的高效合成新方法,先后发展了异色满(Angew.Chem.Int.Ed,2018,57,3444)和1,3-顺式双取代四氢异喹啉(Angew.Chem.Int.Ed.2018,57,10980)的新合成方法,并应用于复杂天然产物(–)-berkelicacid的全合成(Angew.Chem.Int.Ed.2021,60,5141)。在这些研究基础上,该课题组进一步发展了Pd/NBE协同催化与金催化环化/还原的串联反应,只需使用简单易得的三种基础化学品为原料,就可以快速构建出结构多样化的1,3-反式二取代四氢异喹啉化合物。他们应用该方法简洁地合成了药物分子mevidalen的一个类似物,并发展了抗疟活性天然产物korupensamineA和B的5步合成法以及抗HIV活性天然产物michellamineB和C的7步合成法,是迄今最短且最高效的全合成路线。这些高效的合成应用展示了该合成方法在制备1,3-反式四氢异喹啉生物碱及相关药物活性分子方面的巨大潜力。
该研究得到了国家自然科学基金项目、生命有机国家重点实验室开放基金、武汉大学拔尖创新人才培育项目和武汉大学海外人才启动基金的支持。
论文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202205245
(编辑:肖珊)