新闻网讯(通讯员高研院)Nature Cell Biology(《自然•细胞生物学》)近日在线发表了高等研究院刘郑教授课题组在生物物理交叉领域的最新研究成果。课题组设计出一种新型DNA结构的荧光张力探针,并应用于活细胞运动过程的机械力可视化研究。该技术有望成为研究肿瘤细胞迁移、免疫细胞识别和激活等机械力深度参与生命过程的重要工具。
论文题目为“A Reversible shearing DNA probe forvisualizing mechanically strong receptors in living cells”,高等研究院2018级博士研究生李洪云为第一作者,刘郑教授为唯一通讯作者。合作者包括我校生命科学学院张兴华研究员及其团队的博士生张晨、中山大学的马杰教授。第一作者单位为武汉大学。
电学、化学和力学是细胞内最常见的三大信号系统,它们相互协调,共同维持着细胞的生命活动。前两者已被广泛研究,而细胞的机械力信号传递过程因缺少有效的研究方法,人类对其认识有限。实际上,细胞的生命过程不断地受到挤压、拉伸、弯曲和拉扯细胞外基质等过程产生的机械力所调控。尽管细胞上每个受体上传递的机械力小得令人难以置信---分布在几pN到几十pN范围,但是这些机械力信号可以深刻影响胚胎发育、肿瘤迁移、免疫识别等多种过程。因此,在空间和时间上对细胞机械力进行精准地表征,可以帮助我们深入认识细胞是如何利用微观力学信号诱导和改变相关的生物化学信号。
该工作设计出一种新型DNA结构的荧光张力探针并应用于活细胞运动过程的机械力可视化研究,具有力学量程宽、可逆、单分子灵敏度等优势,并可以用光来控制该探针的机械结构进而达到控制细胞力的功能。通过对细胞迁移过程中整合素介导的机械力进行研究,发现了一类少量、但传递更强机械力的整合素团簇(称“力学热点”)在细胞运动过程扮演着重要角色。该技术有望成为研究肿瘤细胞迁移、免疫细胞识别和激活等机械力深度参与的生命过程的重要工具。
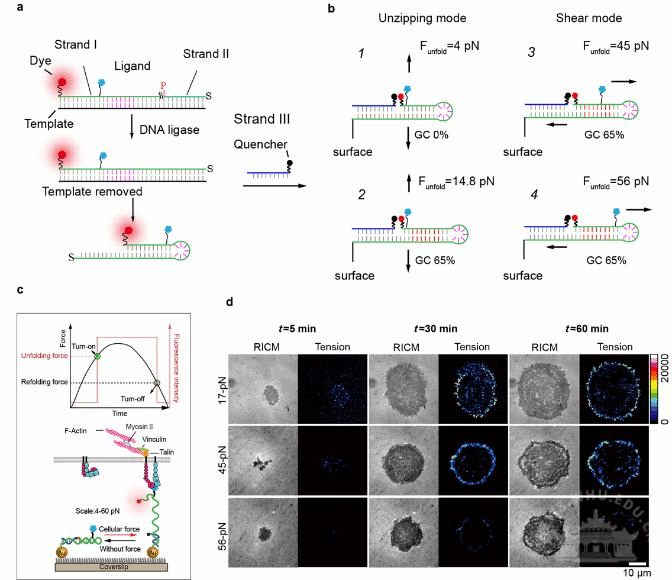
基于新型DNA结构的分子力学探针原理及细胞力学可视化研究
该工作得到了国家自然基金委、武汉大学启动经费以及校内自主科研-学科交叉项目的支持。
据悉,刘郑课题组目前主要从事开发多种高时、空分辨率的分子—细胞力学研究技术,并利用这些技术深入研究机械力在肿瘤迁移、免疫细胞识别和激活等过程中扮演的角色以及分子机制,从新的角度理解肿瘤免疫系统失调的原因,为开发免疫治疗肿瘤方法提供新的理论和技术指导。
论文链接:https://www.nature.com/articles/s41556-021-00691-0
刘郑课题组主页:http://www.liulabwhu.org/
(编辑:付晓歌)