新闻网讯(通讯员强玉龙)近日,我校泰康医学院(基础医学院)李枫教授课题组在肿瘤学主流期刊CancerResearch杂志上在线发表了题为“KDM5C-mediated recruitment of BRD4 to chromatin regulates enhancer activation and BET inhibitor sensitivity”的研究成果。李枫为本研究的通讯作者,泰康医学院(基础医学院)博士研究生强玉龙、范佳宸为本文的共同第一作者。
本研究报道了KDM5C介导的BRD4染色质结合是一种独立于bromodomain的招募方式。另外,作者发现利用KDM5CPROTAC药物联合BETi的联合治疗方式可以有效降低BETi用药浓度,提高肿瘤细胞对BETi的敏感性。
靶向治疗是癌症治疗的主要手段之一,主要通过靶向肿瘤细胞中促癌生物大分子来进行。包括BRD4在内的BET家族蛋白在多种癌症中表达上调,传统上认为它们依靠bromo domain被招募到染色质而促进癌基因表达和推动癌症演进,但是否存在其它招募方式还不是很清楚。有关靶向BET家族蛋白抑制剂(bromo- and extra terminal inhibitors,BETi)的研究一直受到领域内的高度关注。临床试验发现,BETi虽然在癌症治疗中有一定效果,但单一药物治疗所导致的高剂量给药方式会产生严重的毒副作用,并引起癌细胞的耐药。此外,近年来的多项研究表明,基于多靶点的肿瘤联合治疗手段有望降低药物使用剂量和提高治疗效率,从而缓解药物产生的毒副作用,因此开发新型基于BETi的联合治疗手段具有重要的临床意义。

机制上,KDM5C-JmjC功能域通过与BRD4-C末端相互作用,将BRD4招募到增强子上,并且这种招募并不依赖于KDM5C的组蛋白去甲基化酶活性;同时,BRD4-C末端结合KDM5C-JmjC功能域可有效促进KDM5C组蛋白去甲基化酶活性,使得KDM5C在增强子上能够维持高H3K4me1水平,调控增强子活性。此外,研究人员使用KDM5C-PROTAC药物结合JQ1等BETi药物同时靶向KDM5C和BRD4蛋白,并在细胞、动物以及类器官水平验证了这种方法的靶向治疗效果,对BETi在临床上的应用提供了有价值的线索。
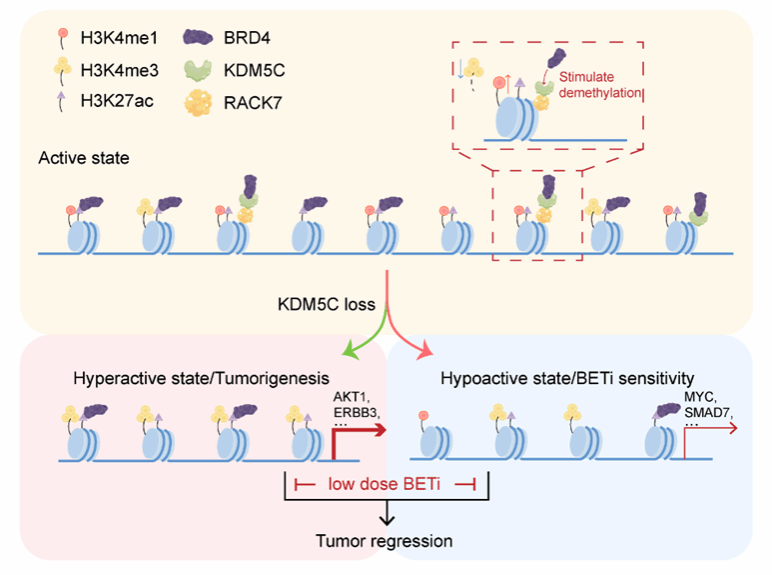 KDM5C介导的BRD4染色质招募和与之相应的靶向治疗策略
KDM5C介导的BRD4染色质招募和与之相应的靶向治疗策略
泰康医学院(基础医学院)梁凯威和魏蕾教授,武汉大学中南医院张蔚、刘羽主任,以及中国科学院精密测量研究院陈世祯研究员为本研究提供了帮助。本研究受到国家自然科学基金、湖北省创新群体等项目的资助。
据悉,李枫课题组长期从事癌症靶向治疗研究,近年来以独立或者主要通讯作者在CancerResearch(2018,2019,2024), Nature Communications(2024), Cell Reports (2023,2023),Oncogene (2023)等杂志发表了一系列研究成果。
原文链接:https://doi.org/10.1158/0008-5472.CAN-23-2888
(学生编辑:陈巧燕 编辑:肖珊)