新闻网讯(通讯员董美玲)5月25日,武汉大学生命科学学院、泰康生命医学中心、免疫与代谢前沿科学中心陈学峰教授课题组在Nature Communications杂志上发表了题为“Bre1/RNF20 promotes Rad51-mediated strand exchange and antagonizes the Srs2/FBH1 helicases”的研究成果,该研究发现并证明了泛素连接酶Bre1/RNF20具有同源重组中介蛋白(recombination mediator)的重要功能。武汉大学为第一作者单位,生命科学学院2017级博士研究生刘光学(现为浙江大学附属第一医院副研究员)和2020级博士研究生李济民是论文共同第一作者,生命科学学院陈学峰教授为通讯作者。

本课题组之前研究发现酵母泛素E3连接酶Bre1通过与ssDNA结合蛋白RPA相互作用被招募到染色质上复制叉处或DNA损伤位点,促进局部染色质上H2B发生泛素化修饰,从而促进DNA复制和修复(Zheng et al., Nucleic Acids Res, 2018; Liu et al., PNAS,2021)。在本研究中,作者揭示Bre1及其人类同源蛋白RNF20能够通过不依赖于泛素连接酶活性的方式来促进同源重组修复,发挥重组中介蛋白的功能。利用质谱和生化技术,作者发现酵母Bre1与重组酶Rad51之间存在直接相互作用,并确定了Bre1中氨基酸E500及K502是介导二者互作的关键位点。特异性破坏二者互作(bre1-EK2A)导致细胞同源重组效率降低以及对DNA损伤试剂敏感,并且证明bre1-EK2A突变不影响其E3连接酶活性。
结合生化和单分子技术,一方面,作者发现Bre1-Rad51互作有助于Rad51替代结合在ssDNA上的RPA,促进Rad51-ssDNA核蛋白丝组装与稳定,并促进Rad51介导的链交换反应;另一方面,作者发现Bre1与反重组酶Srs2存在依赖于ssDNA的相互作用,且该互作促进Srs2从ssDNA上解离。这样,Bre1通过拮抗Srs2进一步保护Rad51-ssDNA免受Srs2的破坏作用。进一步,作者验证了这种机制的保守性。在人类细胞中,作者发现肿瘤抑制因子RNF20 (Bre1同源蛋白)与hRad51存在直接互作,并且能够促进hRad51结合ssDNA,促进hRad51替换ssDNA上的RPA。同样,RNF20也能够与反重组酶FBH1互作,并拮抗FBH1对hRad51-ssDNA核蛋白丝的破坏作用。
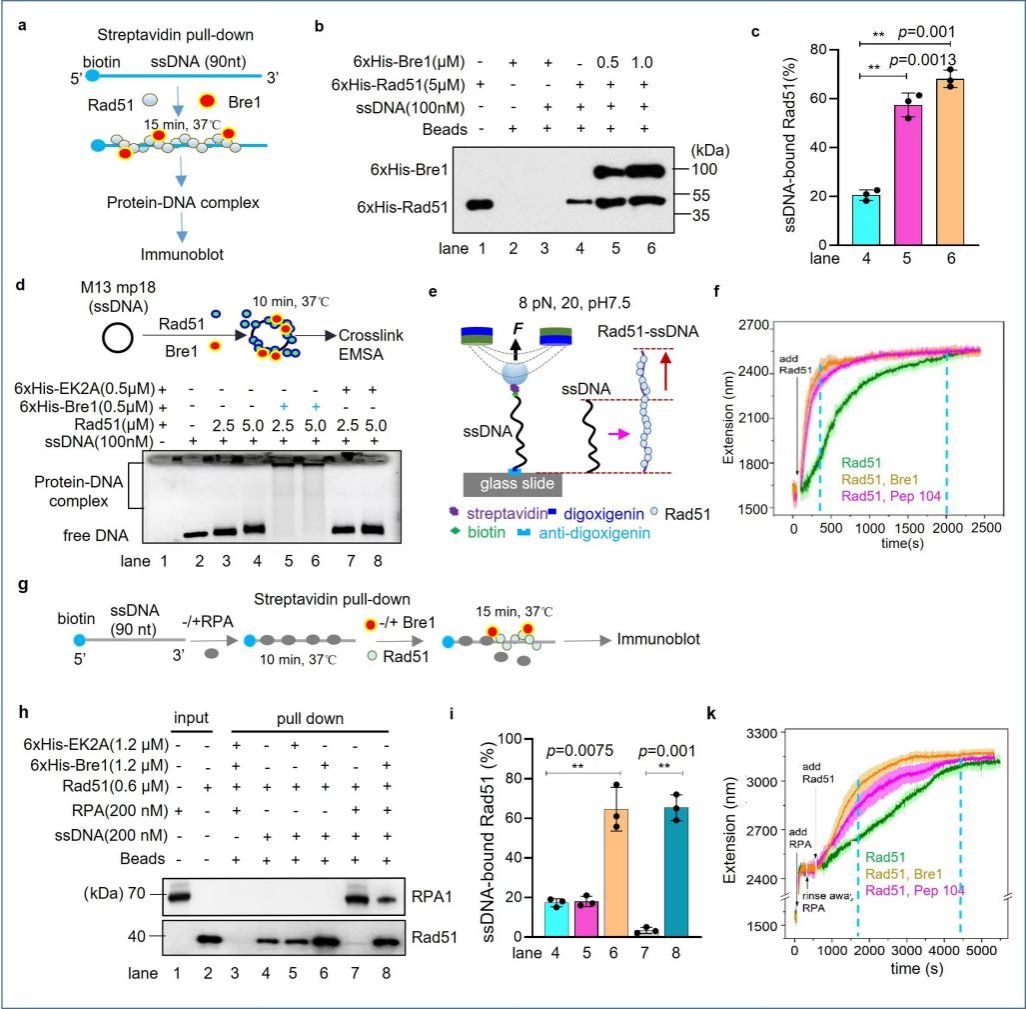
图1:Bre1/RNF20促进Rad51-ssDNA组装及替换RPA
结合过去的研究报道,作者提出Bre1/RNF20在同源重组修复过程中发挥两方面的功能:第一,Bre1/RFN20作为E3连接酶促进染色质局部H2B泛素化响应DNA修复;第二,Bre1/RFN20通过独立于E3连接酶活性的方式,发挥同源重组中介蛋白的功能,从而促进DNA重组修复。该项研究深化了我们对同源重组修复调控机理的认识,揭示了肿瘤抑制因子RNF20在维持基因组稳定性中重要新功能。
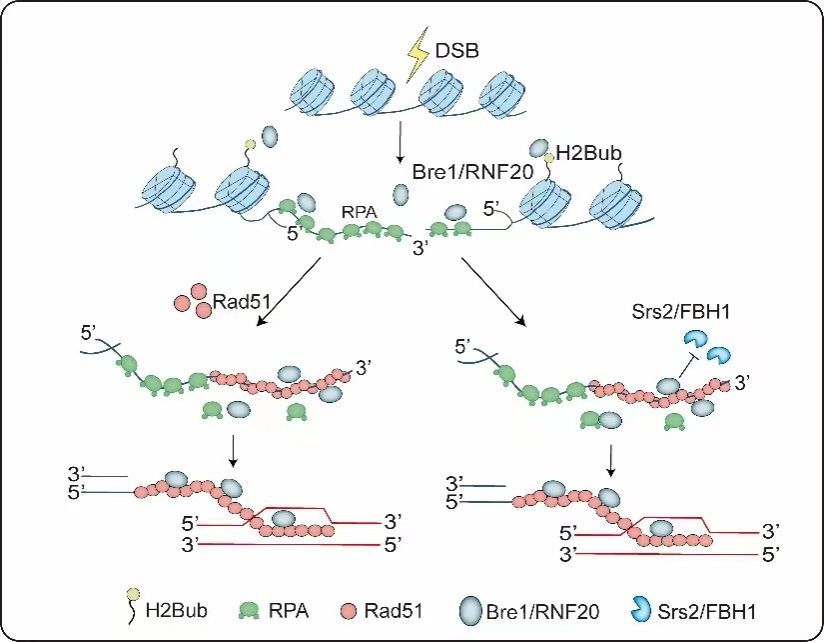
图2:Bre1/RNF20促进同源重组修复分子机制模型
生命科学院张兴华教授、浙江大学周春教授、南京大学附属鼓楼医院许景艳教授、武汉大学人民医院李祥攀教授参与了该项研究。据悉,该项研究工作得到了国家重点研发计划项目、国家自然科学基金面上项目和武汉大学泰康生命医学中心的经费支持。
论文链接:https://www.nature.com/articles/s41467-023-38617-z
(实习编辑:师捷 编辑:张丽平)