新闻网讯(通讯员杨雪)1月17日,国际期刊《Nature Communications》(IF=12.353)在线发表了武汉大学生命科学学院宋保亮教授实验室的最新研究成果,论文题为“Competitive oxidation and ubiquitylation on the evolutionarily conserved cysteine confer tissue-specific stabilization of Insig-2”(保守半胱氨酸的竞争性氧化与泛素化修饰确保Insig-2在特定的组织中稳定)。该工作发现脂代谢调控蛋白Insig-2的泛素化位点为半胱氨酸Cys,后者可被肌肉细胞内活性氧(ROS)氧化而稳定,从而防止肌肉细胞内脂质的过度累积。该工作揭示细胞通过Cys的竞争性氧化与泛素化而感受ROS,并提示该机制在动物从水生向陆生的进化过程中发挥作用。
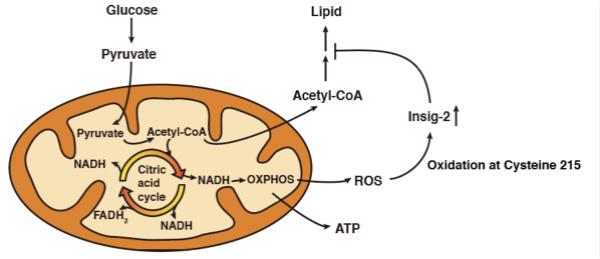
肌肉中活性氧类(ROS)通过Insig-2蛋白调控脂质代谢示意图
肌肉中脂质的过度积累是引起胰岛素抵抗的重要原因。Insig-2是一个负调控脂质生物合成的内质网蛋白,研究人员发现该蛋白Cys215位点既是泛素化修饰位点又是氧化修饰位点,Cys215被氧化后稳定,抑制脂质合成。通过对Insig-2蛋白的进化树分析发现,从水生向陆生的进化过程中,陆生脊椎动物Insig-2蛋白的第215位半胱氨酸变得高度保守。推测陆生脊椎动物肌肉细胞中高ROS含量竞争性氧化Insig-2蛋白C215位点,导致该蛋白泛素化水平降低,从而增加了Insig-2蛋白稳定性。稳定后的Insig-2蛋白进一步抑制SREBP途径并降低肌细胞中脂质合成,促进ATP生成和保护肌肉细胞免受脂质过度积累而影响功能。
这是宋保亮实验室继2017年在Nature Cell Biology首次报道ACAT2蛋白的Cys残基被竞争性氧化与泛素化修饰后,进一步在Insig-2蛋白上发现该机制,这表明Cys的竞争性氧化和泛素化修饰是细胞感受ROS的普遍机制。
宋保亮实验室的周章森博士、博士生李美欣、柳洁为该论文的共同第一作者。宋保亮为通讯作者。该研究的共同作者还包括武汉大学生命科学学院赵华斌教授、罗婕副教授、史熊杰副教授等。该工作得到了国家科技部、国家自然科学基金、教育部111引智基地的资助。
(编辑:阳霖)