新闻网讯(通讯员任艺萱)近日,国际材料学顶级期刊 Advanced Materials(《先进材料》)在线发表武汉大学人民医院徐细明/饶浪团队最新研究成果。该项研究将临床医学、肿瘤生物学与纳米材料交叉结合,把液-液相分离这一新兴生物学过程与肿瘤免疫治疗、纳米药物递送有机融合,提出了兼具机制创新性与应用潜力的新策略,为提升肝细胞癌免疫治疗疗效提供了新的理论依据和技术路径。
论文题为“Disrupting KAT8 Liquid-Liquid Phase Separation with Hybrid Vesicle-Liposome Platform for Enhanced PD-L1 Blockade Treatment”(利用杂化囊泡-脂质体平台破坏KAT8液-液相分离以增强PD-L1阻断治疗)。武汉大学人民医院为第一作者单位和通讯作者单位,第一临床学院2024级博士生胡心瑶、神经外科博士后朱华和深圳湾实验室副研究员孟倩芳为共同第一作者,武汉大学人民医院肿瘤中心徐细明教授与人民医院客座教授、深圳湾实验室饶浪教授为共同通讯作者。
肝细胞癌是我国常见的高致死性恶性肿瘤之一。近年来,PD-1/PD-L1免疫检查点阻断治疗为肝癌治疗带来了新的希望,但临床上仍面临患者应答率有限、肿瘤内药物递送不足以及PD-L1持续转录补充等关键难题。围绕这些问题,徐细明/饶浪团队开展深入研究,发现赖氨酸乙酰转移酶8(KAT8)可作为液-液相分离(LLPS)转录凝聚体的重要驱动因子,通过与IRF1协同形成转录凝聚体,持续维持PD-L1表达并促进肿瘤免疫逃逸。
基于上述发现,研究团队进一步构建了一种PD-1功能化杂化囊泡-脂质体递送材料(PD-1-HVL–siKAT8)。该材料兼具局部PD-L1阻断和KAT8靶向沉默双重作用,一方面通过表面PD-1实现对肿瘤细胞PD-L1的局部阻断,另一方面递送靶向KAT8的小干扰RNA,从源头瓦解维持PD-L1持续表达的相分离凝聚体,实现“表面阻断+源头抑制”的协同干预。
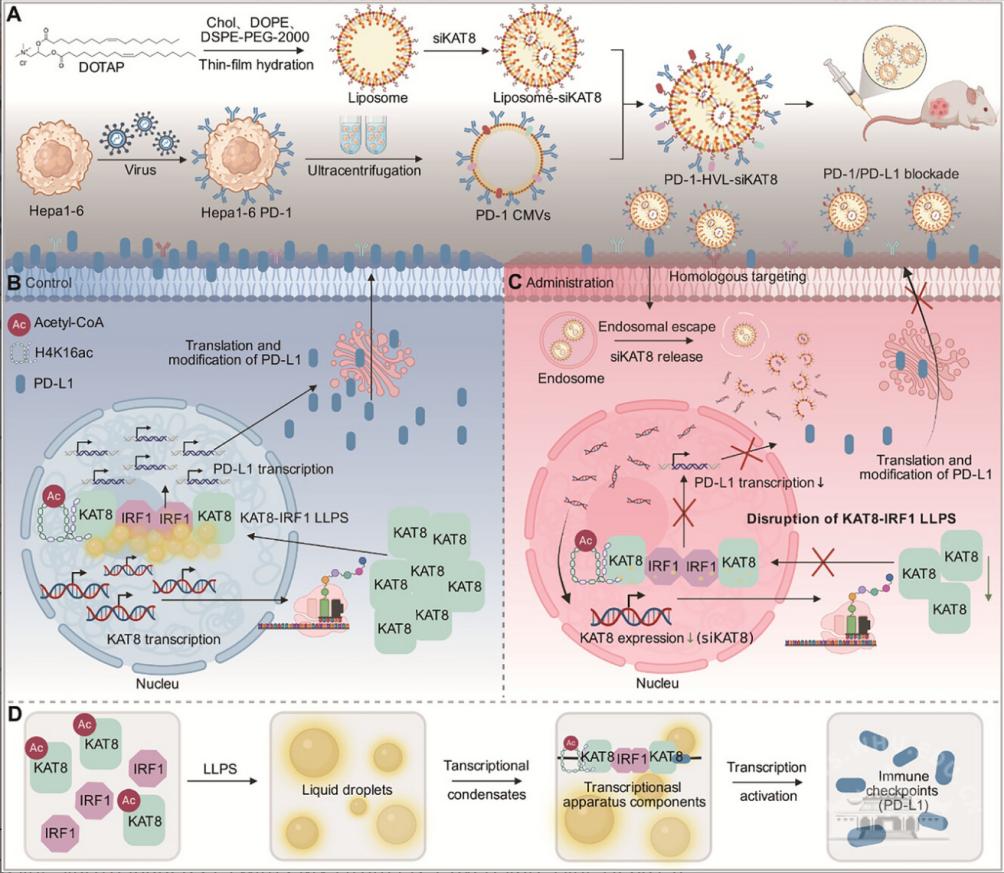
研究表明,该材料可显著抑制PD-L1表达,进一步有效抑制肿瘤生长、延缓术后复发并延长生存期,具有较好的治疗潜力和临床转化前景。
该研究获得国家自然科学基金、湖北省自然科学基金、深圳医学研究基金、广东省基础与应用基础研究基金等项目支持。
论文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.202523584