新闻网讯(通讯员任艺萱)近日,国际化学领域期刊《德国应用化学国际版》(Angewandte Chemie International Edition)在线发表武汉大学人民医院(湖北省人民医院)泌尿外科教授程帆团队与武汉大学药学院合作的最新研究成果。该研究在国际上首次系统地将PROTAC介导的蛋白降解与纳米酶诱导的铁死亡相结合,为攻克去势抵抗性前列腺癌(CRPC)耐药性提供了新的思路,并为纳米PROTAC的临床转化奠定了基础。
论文题为“Nanozyme-Mediated PROTACs Delivery for Targeted Protein Degradation and Ferroptosis Sensitization in Prostate Cancer”(《纳米酶介导的PROTAC递送用于前列腺癌中的靶向蛋白降解与铁死亡增敏》)。武汉大学博士研究生王陈媛、江雪、雷嘉鹏为共同第一作者,程帆、人民医院泌尿外科副教授刘凌琪、药学院教授黎威为共同通讯作者。
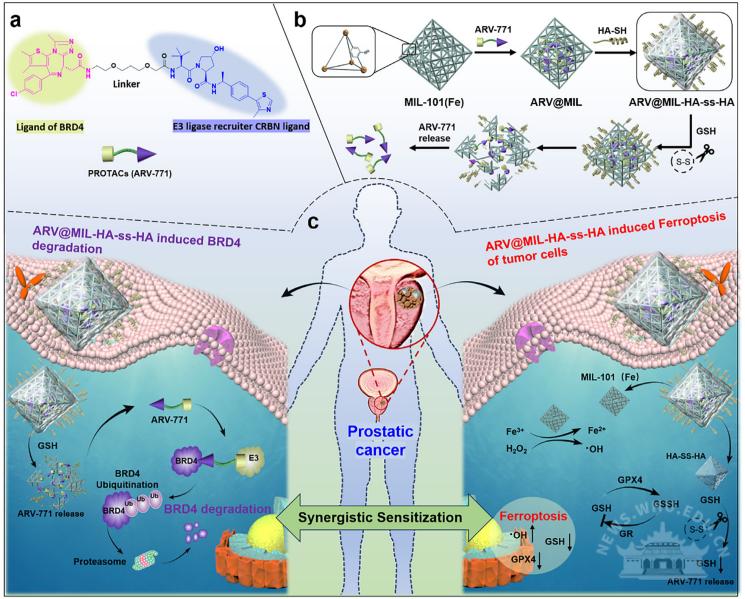
去势抵抗性前列腺癌(CRPC)是当前前列腺癌治疗中的主要临床挑战,尽管AR拮抗剂在一定程度上改善了患者预后,但耐药性几乎不可避免。近年来,蛋白靶向降解嵌合体(PROTAC)药物如ARV-771,通过诱导BRD4蛋白降解,可有效抑制AR/AR-V7的转录活性,展现出良好的治疗潜力。然而,该类药物存在水溶性差、体内稳定性低、靶向性不足等问题,限制了其临床转化。与此同时,铁基MOF材料MIL-101不仅可作为药物载体,还具备类过氧化物酶(POD)和过氧化氢酶(CAT)活性,能够通过催化肿瘤微环境中的H₂O₂生成羟基自由基(·OH)并消耗谷胱甘肽(GSH),从而诱导肿瘤细胞铁死亡。因此,若能将ARV-771与MIL-101结合,并赋予其主动靶向与响应性释放能力,有望实现PROTAC介导的靶向蛋白降解与铁死亡的协同增效,为CRPC治疗提供新策略。
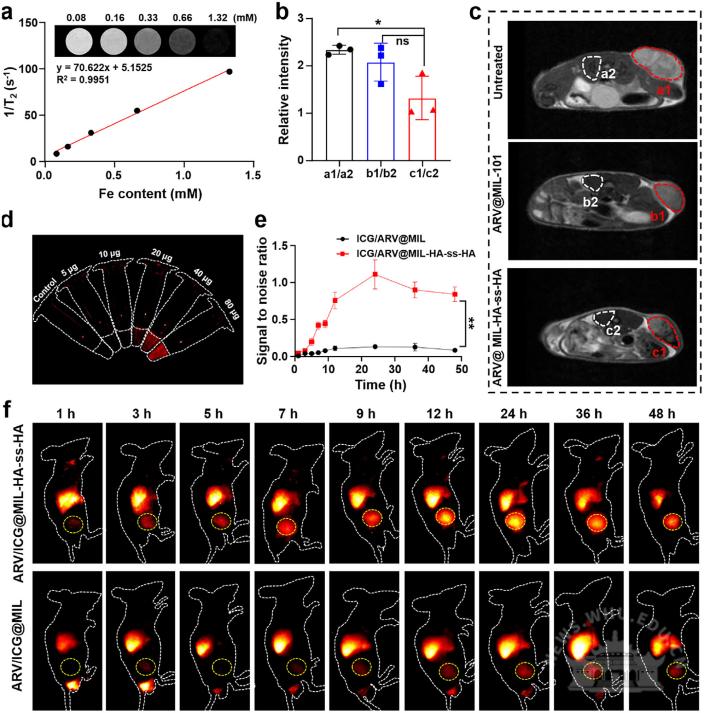
研究设计并构建了一种多功能纳米PROTAC平台ARV@MIL-HA-ss-HA,其核心思路是利用铁基MOF MIL-101作为载体负载ARV-771,并在表面修饰由二硫键交联的透明质酸(HA-ss-HA)水凝胶。该水凝胶一方面通过HA与肿瘤细胞高表达的CD44受体相互作用实现主动靶向,另一方面在肿瘤细胞内高GSH环境中发生二硫键断裂,触发药物响应性释放。MIL-101载体本身可作为纳米酶,在肿瘤细胞内催化H₂O₂生成·OH并消耗GSH,诱导铁死亡;同时释放的ARV-771通过降解BRD4蛋白,既直接抑制肿瘤生长,又进一步增强细胞对铁死亡的敏感性,从而实现双重协同治疗。研究通过体外细胞实验、蛋白组学分析、体内肿瘤模型、MRI与荧光成像等手段,系统评估了该纳米平台的靶向性、药物释放特性、BRD4降解能力、铁死亡诱导效应、抗肿瘤疗效及生物安全性。
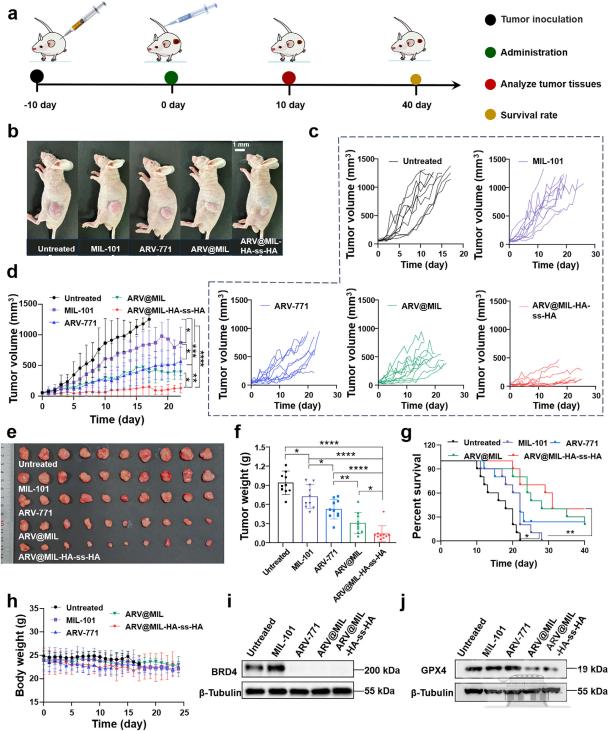
研究证实,该新型纳米PROTAC平台ARV@MIL-HA-ss-HA,可通过将铁基MOF MIL-101的纳米酶活性与PROTAC药物ARV-771的靶向蛋白降解功能相结合,实现对CRPC的高效协同治疗。体外与体内实验均证实,该策略显著提高了药物的肿瘤富集、BRD4降解效率、铁死亡诱导能力及抗肿瘤疗效,同时展现出良好的生物安全性。本项研究首次系统地将PROTAC介导的蛋白降解与纳米酶诱导的铁死亡相结合,为克服CRPC耐药性提供了新的思路,并为纳米PROTAC的临床转化奠定了基础。
该研究得到国家自然科学基金和湖北省自然科学基金的支持。
论文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.6657773